

华蓥的高级中学可以开复读班相关问题汇总
1、高考可复读?
2、公办学校复读?
3、高三可以复读吗?
4、2022高考生能不能复读?
5、高中可不可以复读?

华蓥的高级中学可以开复读班入学检测化学选择题摘录
1、下列关于热化学反应的描述中正确的是( )
A.HCI和NaOH反应的中和热ΔH=-57.3kJ/mol,则H2SO4和Ca(OH) 2反应的中和热△H=2×(-57.3)KJ/mol
B.CO(g)的燃烧热是283.0kJ/mol,则2CO2 (g)=2C![]() O(g)+O2 (g)反应的
O(g)+O2 (g)反应的![]()
△H=+2×283.0kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
【知识点】燃烧热和中和热
【答案】
B
2、下列排列顺序不正确的是
A.热稳定性:HF>H2O>NH3 B.原子半径:Cl>S>P
C.碱性:NaOH>Mg(OH)2>Al(OH)3 D.金属性:K>Na>Li
【知识点】物质结构 元素周期律单元测试
【答案】
【答案】B
【解析】
试题分析:A、非金属性越强,其氢化物越稳定,非金属性的强弱:F>O>N,因此氢化物的稳定性是HF>H2O>NH3,故说法正确;B、同周期从左向右半径减小,稀有气体除外,因此是P>S>Cl,故说法错误;C、最高价氧化物对应水化物的碱性越强,其金属性越强,反之也成立,根据金属活动顺序表,金属性:Na>Mg>Al,碱性:NaOH>Mg(OH)2>Al(OH)3,故说法正确;D、同主族从上到下,金属性增强,金属性:K>Na>Li,故说法正确。
考点:考查元素的性质等知识。
3、在恒温条件下,向盛有食盐的2L恒容密闭容器中加入0.2molNO2、0.2molNO和0.1molCl2,发生如下两个反应:
①2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g)△H1<0 平衡常数K1
②2NO(g)+Cl2(g)⇌2ClNO(g)△H2<0 平衡常数K2
10min时反应达到平衡,测得容器内体系的压强减少20%,10min内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10﹣3mol/(L•min).下列说法不正确的是( )
A.反应4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数为K12/K2
B.平衡后c(Cl2)=2.5×10﹣2mol/L
C.其它条件保持不变,反应在恒压条件下进行,则平衡常数K2增大
D.平衡时NO2的转化率为50%
【知识点】化学平衡
【答案】
【考点】CP:化学平衡的计算.
【分析】A.①2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g),平衡常数K1=![]()
![]() ,
,
②2NO(g)+Cl2(g)⇌2ClNO(g),平衡常数K2 =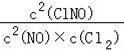
 ,
,
2×①﹣②可得4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g),进而计算平衡常数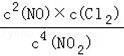
 ;
;
B.10min时反应达到平衡,测得容器内体系的压强减少20%,则平衡时混合气体总物质的量为(0.2+0.2+0.1)mol×(1﹣20%)=0.4mol,10min内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10﹣3mol•L•min﹣1,则平衡时n(ClNO)=7.5×10﹣3mol•L•min﹣1×10min×2L=0.15mol,设①中反应的NO2为xmol,②中反应的Cl2为ymol,则:
2NO2(g)+NaCl(s)═NaNO3(s)+ClNO(g)
xmol 0.5xmol
2NO(g)+Cl2(g)═2ClNO(g)
2ymol ymol 2ymol
再根据ClNO物质的量与平衡时混合气体总物质的量列方程计算解答;
C.平衡常数只受温度影响,温度不变,则为平衡常数不变;
D.根据C中的计算结果,可以计算二氧化氮的转化率.
【解答】解:A.①2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g),平衡常数K1=![]()
![]() ;
;
②2NO(g)+Cl2(g)⇌2ClNO(g),平衡常数K2 =

4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=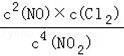
 ,
,
则[![]()
![]() ]2÷
]2÷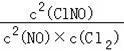
 =
=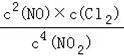
 ,即K=
,即K=![]()
![]() ,故A正确;
,故A正确;
B.10min时反应达到平衡,测得容器内体系的压强减少20%,则平衡时混合气体总物质的量为(0.2+0.2+0.1)mol×(1﹣20%)=0.4mol,10min内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10﹣3mol•L•min﹣1,则平衡时n(ClNO)=7.5×10﹣3mol•L•min﹣1×10min×2L=0.15mol,设①中反应的NO2为xmol,②中反应的Cl2为ymol,则:
2NO2(g)+NaCl(s)═NaNO3(s)+ClNO(g)
xmol 0.5xmol
2NO(g)+Cl2(g)═2ClNO(g)
2ymol ymol 2ymol
则0.5x+2y=0.15,(0.2﹣x+0.2﹣2y+0.1﹣y)+0.5x+2y=0.4,联立方程,解得x=0.1、y=0.05,
故平衡后c(Cl2)=![]()
![]() =2.5×10﹣2mol•L﹣1,故B正确;
=2.5×10﹣2mol•L﹣1,故B正确;
C.平衡常数只受温度影响,其他条件保持不变,反应在恒压条件下进行,则平衡常数K2不变,故C错误;
D.平衡时NO2的转化率为![]()
![]() ×100%=50%,故D正确,
×100%=50%,故D正确,
故选C.

华蓥的高级中学可以开复读班入学检测英语选择题摘录
1、 China can _______ a global role in improving public health by sharing some of its vaccines (疫苗) with other developing countries.
A. take effect B. fix up C. take on D. pile up
【知识点】词组 短语 【答案】
C
2、 You should have prepared your speech for the meeting , Mr. Smith .
Yes , I know . But how could I do____ the meeting date fixed so soon?
A.while B.as C.after D.with
【知识点】独立主格结构 with的复合结构 【答案】
D
解析:with复合结构,表示原因。
3、 — Do you want tea or coffee?
— I don’t mind, ______ one you’re making.
A.however B.whenever C.whichever D.whatever
【知识点】形容词 【答案】
C
4、 You might wonder how this kind of animal ____ to live without eating for so many months. A.keeps B.succeeds C.manages D.tries
【知识点】其他 【答案】
C
关于华蓥的高级中学可以开复读班相关信息,小编就整理到这里,感谢大家一如既往的支持,如有其它问题需要咨询,请直接联系我们。
