

宜宾高中生如何复读相关问题汇总
1、高考怎样复读?
2、高中复读书政策?
3、今年省公办性高中不再招收复读生吗?
4、今年还可以复读高三不?
5、高三复读条件?

宜宾高中生如何复读入学检测化学选择题摘录
1、下列有关说法正确的是
A. 25℃时NH4Cl溶液的Kw大于100℃时NaCl溶液的Kw
B. pH=2的盐酸和pH=12的NaOH溶液等体积混合后溶液肯定呈中性
C. 将常温下0.1 mol/L pH=a的醋酸稀释到pH=a+1时,其物质的量浓度c<0.01 mol/L
D. 等体积等pH的盐酸和醋酸与足量锌反应时,开始时反应速率相等,最终产生的氢气一样多
【知识点】电离平衡单元测试
【答案】
【答案】C
【解析】
【详解】A. 25℃时NH4Cl、NaCl均为强电解质,不存在电离平衡,A错误;
B.常温时,pH=2的盐酸和pH=12的NaOH溶液等体积混合后溶液肯定呈中性,未给定温度,则不一定为中性,B错误;
C. 将常温下0.1 mol/L pH=a的醋酸稀释到pH=a+1时,加水稀释后的体积大于原来的10倍,其物质的量浓度c<0.01 mol/L,C正确;
D. 等体积等pH的盐酸和醋酸与足量锌反应时,开始时反应速率相等,醋酸为弱电解质,随反应的进行,未电离的分子逐渐电离,最终产生的氢气比盐酸多,D错误;
答案为C
【点睛】醋酸为弱电解质,加水稀释时,未电离的分子逐渐电离,导致氢离子浓度减小的程度小,稀释为原来氢离子浓度的1/10时,则需多加水。
2、25℃时,用0.100 mol·L-1的NaOH溶液滴定20.00 mL 0.100 mol·L-1的HNO2溶液,![]() 与所加NaOH溶液体积的关系如图所示,下列说法错误的是( )
与所加NaOH溶液体积的关系如图所示,下列说法错误的是( )
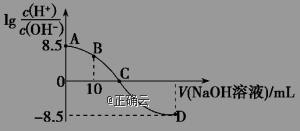
A.25 ℃时,0.100 mol·L-1的HNO2溶液的pH=2.75
B.B点对应的溶液中,2c(H+)+c(HNO2)=c(NO2-)+2c(OH-)
C.C点对应的溶液的pH=7,加入NaOH溶液的体积为20.00 mL
D.滴定过程中从A到D点溶液中水的电离程度先增大后减小
【知识点】电离平衡 水解平衡
【答案】
C
3、取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,同温
同压下放出相同体积的气体,则两份铝片的质量之比为( )
A.1:6 B.2:3 C.3:2 D. 1:1
【知识点】镁和铝
【答案】
D

宜宾高中生如何复读入学检测英语选择题摘录
1、 When you come here for your holiday next time, don’t go to ___ hotel; I can find you ____
bed in my flat.
A. the; a B. the; / C. a; the D. a; /
【知识点】语法 【答案】
A
2、 When people choose what college course to take, _____question tends to be: what kind of ____job am I going to get?
A./; / B.the; / C./; a D.the; the
【知识点】冠词 【答案】
B
3、 A clean environment can help the city bid for the Olympics, which _______ will promote its economic development.
A. in nature B. in return C. in turn D. in fact
【知识点】介词 介词短语 【答案】
C
4、 His parents wouldn’t let him marry anyone ____ family was poor.
A. of whom B. whom C. of whose D. whose
【知识点】复合句 【答案】
D
关于宜宾高中生如何复读相关信息,小编就整理到这里,感谢大家一如既往的支持,如有其它问题需要咨询,请直接联系我们。
