

攀枝花高考后如何复读相关问题汇总
1、今年届高考生能否复读?
2、高考如何复读?
3、哪里可以复读高三?
4、高考录取后可以复读吗?
5、高中能不能复读?

攀枝花高考后如何复读入学检测化学选择题摘录
1、25℃时,弱酸的电离平衡常数如表所示,下列说法正确的是( )
| 弱酸 | CH3COOH | HCN | H2CO3 |
| Ka | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
A.0.1 mol/L 的CH3COOH的 pH比0.1mol/L HCN的pH大
B.等物质的量浓度溶液pH关系:pH(CH3COONa)<pH(NaHCO3) <pH(NaCN)
C.向NaCN溶液中通入少量CO2: CO2 + H2O + 2NaCN == 2HCN + Na2CO3
D.NaHCO3和Na2CO3的混合液中:c(Na+) +c(H+)=c(OH-)+ c(HCO3-)+c(CO32-)
【知识点】电离平衡单元测试
【答案】
B
2、已知弱酸的电离平衡常数如下表,下列选项正确的是( )
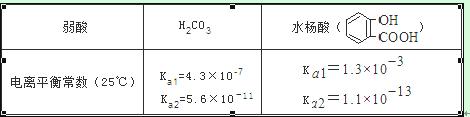
A.常温下,等浓度、等体积的NaHCO3 溶液pH小于![]() 溶液pH
溶液pH
B.常温下,等浓度、等体积的Na2 CO3 溶液和 ![]() 溶液中所含离子总数前者小于后者
溶液中所含离子总数前者小于后者
C.![]()
D.水杨酸的第二级电离 Ka2 远小于第一级电离Ka1 的原因之一是 能形成分子内氢键
【知识点】电离平衡单元测试
【答案】
D
3、Cl2是纺织工业中常用的漂白剂,Na2S2O3可作为漂白布匹后的“脱氯剂”。S2O![]() 和Cl2反应的产物之一为SO
和Cl2反应的产物之一为SO![]() 。下列说法中,不正确的是( )
。下列说法中,不正确的是( )
A.该反应中氧化剂是Cl2
B.根据该反应可判断还原性:S2O![]() >Cl-
>Cl-
C.上述反应中,每生成1 mol SO![]() ,可脱去2 mol Cl2
,可脱去2 mol Cl2
D.SO2与氯气的漂白原理相同,所以也可以用SO2做纺织工业的漂白剂
【知识点】氧化还原反应
【答案】
答案 D
解析 S2O![]() 和Cl2反应的产物之一为SO
和Cl2反应的产物之一为SO![]() ,S元素的化合价升高,则Cl元素的化合价降低,因Cl元素的化合价降低,所以氧化剂是Cl2,故A正确;由还原剂的还原性大于还原产物的还原性可知,还原性:S2O
,S元素的化合价升高,则Cl元素的化合价降低,因Cl元素的化合价降低,所以氧化剂是Cl2,故A正确;由还原剂的还原性大于还原产物的还原性可知,还原性:S2O![]() >Cl-,故B正确;每生成1 mol SO
>Cl-,故B正确;每生成1 mol SO![]() ,由电子守恒可知,转移4 mol电子,则可脱去2 mol Cl2,故C正确;SO2与氯气的漂白原理不相同,氯气是利用其氧化性,而二氧化硫是利用化合反应,故D错误。
,由电子守恒可知,转移4 mol电子,则可脱去2 mol Cl2,故C正确;SO2与氯气的漂白原理不相同,氯气是利用其氧化性,而二氧化硫是利用化合反应,故D错误。

攀枝花高考后如何复读入学检测英语选择题摘录
1、 He joined the army in the year ____ the Anti-Japanese War broke out.
A. when B. which C. in that D. during which
【知识点】定语从句 【答案】
A2、It is our desire that every effort _______ to protect the surroundings in our school.
A.is made B.was made C.be made D.will make
【知识点】虚拟语气与情态动词 【答案】
C
3、 With most of the problems _____, I felt a great weight taken off my mind.
A. to solve B. solved C. solving D. being solved
【知识点】非谓语动词 【答案】
B
4、 The government's strong action demonstrated its _____ to crush the rebellion.
A. energy B. resistance C. courage D. determination
【知识点】名词 【答案】
D. determination.
解析:determination意为“决心”, 后常接动词不定式作定语。
关于攀枝花高考后如何复读相关信息,小编就整理到这里,感谢大家一如既往的支持,如有其它问题需要咨询,请直接联系我们。
